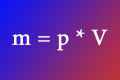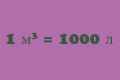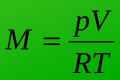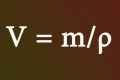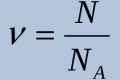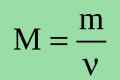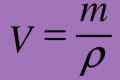Як знайти об'єм газу?

Перш ніж вирішувати завдання, слід занть формули і правила того, як знайти об`єм газу. Слід згадати закон Авогадро. А сам обсяг газу можна обчислити за допомогою декількох формул, вибравши з них відповідну. При підборі необхідної формули, велике значення мають умови середовища, зокрема температура і тиск.
закон Авогадро
У ньому говориться, що при однаковому тиску і однаковою температурі, в одних і тих же обсягах різних газів, буде міститися однакове число молекул. Кількість молекул газу, що містяться в одному молі, це є число Авогадро. З цього закону випливає, що: 1 кмоль (кіломоль) ідеального газу, причому будь-якого, при тому самому тиску і температурі (760 мм рт.ст. і t = 0 * С) завжди займає один обсяг = 22,4136 м3.
Як визначити обсяг газу
- Формулу V = n * Vm найчастіше можна зустріти в задачах. Тут обсяг газу в літрах - V, Vm - об`єм газу молярний (л / моль), який за нормальних умов = 22,4 л / моль, а n - кількість речовини в молях. Коли в умовах немає кількості речовини, але при цьому є маса речовини, тоді чинимо таким чином: n = m / M. Тут М - г / моль (молярна маса речовини), а маса речовини в грамах - m. У таблиці Менделєєва вона написана під кожним елементом, як його атомна маса. Складемо всі маси і отримаємо шукану.
- Отже, як розрахувати обсяг газу. Ось завдання: в соляній кислоті розчинити 10 г алюмінію. Питання: скільки водню може виділитися при н. у.? Рівняння реакції виглядає так: 2Al + 6HCl (хат.) = 2AlCl3 + 3H2. На самому початку знаходимо алюміній (кількість), який вступив в реакцію за формулою: n (Al) = m (Al) / M (Al). Масу алюмінію (молярна) візьмемо з таблиці Менделєєва M (Al) = 27г / моль. Підставами: n (Al) = 10/27 = 0,37моль. З хімічного рівняння видно, 3 молі водню утворилися при розчиненні 2-х молей алюмінію. Слід розрахувати, а скільки ж водню виділиться з 0,4 молі алюмінію: n (H2) = 3 * 0,37 / 2 = 0,56моль. Підставами дані в формулу і знайдемо обсяг цього газу. V = n * Vm = 0,56 * 22,4 = 12,54л.